Estudia los intercambios de energía térmica entre sistemas y los fenómenos mecánicos y químicos que implican tales intercambios. En particular, estudia los fenómenos en los que existe transformación de energía mecánica en térmica o viceversa.Específicamente, la termodinámica se ocupa de las propiedades macroscópicas (grandes, en oposición a lo microscópico o pequeño) de la materia, especialmente las que son afectadas por el calor y la temperatura, así como de la transformación de unas formas de energía en otras.
Cuando la energía (mecánica, térmica, eléctrica, química…) se transforma de una forma a otra, siempre hay una cantidad que se convierte en calor.
Aproximadamente, calor significa "energía en tránsito" y dinámica se refiere al "movimiento", por lo que, en esencia, la termodinámica estudia la circulación de la energía y cómo la energía infunde movimiento.
Históricamente, la termodinámica se desarrolló a partir de la necesidad de aumentar la eficiencia de las primeras máquinas de vapor.
Es importante saber que la termodinámica estudia los sistemas que se encuentran en equilibrio. Esto significa que las propiedades del sistema —típicamente la presión, la temperatura, el volumen y la masa, que se conocen como variables termodinámicas— son constantes.
Además, la termodinámica nos ayuda a comprender por qué los motores no pueden ser nunca totalmente eficientes y por qué es imposible enfriar nada hasta el cero absoluto, una temperatura a la que las sustancias no tienen energía calórica.
Los principios de la termodinámica se pueden aplicar al diseño de motores, al cálculo de la energía liberada en reacciones o a estimar la edad del Universo.
LEYES DE LA TERMODINÁMICA:
***LEY CERO DE LA TERMODINÁMICA.
***LEY PRIMERA DE LA TERMODINÁMICA.
Esta primera ley, y la más importante de todas, también conocida como principio de conservación de la energía, dice: "La energía no puede ser creada ni destruida, sólo puede transformarse de un tipo de energía en otro".
La primera ley de la termodinámica da una definición precisa del calor, y lo identifica como una forma de energía. Puede convertirse en trabajo mecánico y almacenarse, pero no es una sustancia material.
Experimentalmente se demostró que el calor, que originalmente se medía en unidades llamadas calorías, y el trabajo o energía, medidos en julios, eran completamente equivalentes. Una caloría equivale a 4,186 julios.
***LEY SEGUNDA DE LA TERMODINÁMICA.
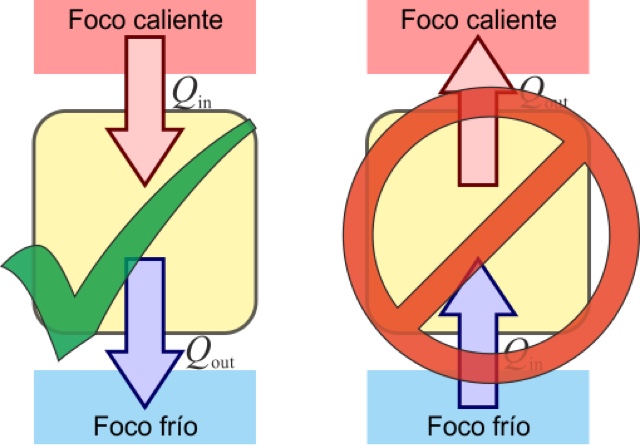
La segunda ley dice que "solamente se puede realizar un trabajo mediante el paso del calor de un cuerpo con mayor temperatura a uno que tiene menor temperatura". Al respecto, siempre se observa que el calor pasa espontáneamente de los cuerpos calientes a los fríos hasta quedar a la misma temperatura.
La segunda ley de la termodinámica da, además, una definición precisa de una propiedad llamada entropía (fracción de energía de un sistema que no es posible convertir en trabajo).
Para entenderla, la entropía puede considerarse como una medida de lo próximo o no que se halla un sistema al equilibrio; también puede considerarse como una medida del desorden (espacial y térmico) del sistema.
Pues bien, esta segunda ley afirma que "la entropía, o sea, el desorden, de un sistema aislado nunca puede decrecer. Por tanto, cuando un sistema aislado alcanza una configuración de máxima entropía, ya no puede experimentar cambios: ha alcanzado el equilibrio".
Como la entropía nunca puede disminuir, la naturaleza parece pues "preferir"’ el desorden y el caos. Puede demostrarse que el segundo principio implica que, si no se realiza trabajo, es imposible transferir calor desde una región de temperatura más baja a una región de temperatura más alta.
***LEY TERCERA DE LA TERMODINÁMICA.
El tercer principio de la termodinámica afirma que "el cero absoluto no puede alcanzarse por ningún procedimiento que conste de un número finito de pasos. Es posible acercarse indefinidamente al cero absoluto, pero nunca se puede llegar a él".
Es importante recordar que los principios o leyes de la Termodinámica son sólo generalizaciones estadísticas, válidas siempre para los sistemas macroscópicos, pero inaplicables a nivel cuántico.
Asimismo, cabe destacar que el primer principio, el de conservación de la energía, es una de las más sólidas y universales de las leyes de la naturaleza descubiertas hasta ahora por la ciencia.




No hay comentarios:
Publicar un comentario